Criteri di scelta del combustibile
4.1 Introduzione
Questa sezione si pone come obiettivo l'individuazione delle possibili scelte tra i sistemi di produzione di idrogeno ovvero dei sistemi di stoccaggio dello stesso a bordo di un veicolo.
Se da un lato la scelta del tipo di tecnologia da utilizzare per le celle è ormai universalmente ricaduta sulle polimeriche, per quanto riguarda l'approvvigionamento dell'idrogeno con cui alimentare il dispositivo esiste tuttora una grande incertezza da parte dei responsabili delle attività di ricerca e sviluppo.
E' possibile identificare due diverse scelte progettuali a soluzione del problema:
· produrre l'idrogeno tramite impianti stazionari e successivamente immagazzinarlo a bordo;
· produrre l'idrogeno, just in time, direttamente all'interno del veicolo partendo da un idrocarburo.
La prima ipotesi che si potrebbe realizzare, sicuramente più semplice per la gestione complessiva del veicolo elettrico, è fortemente vincolata dall'assenza di una tecnologia matura in grado di garantire l'immagazzinamento di grosse quantità di idrogeno in modo conveniente, sicuro e soprattutto con il minor ingombro e peso possibile.
La seconda presenta grosse complicazioni impiantistiche poiché si tratterebbe di installare un reformer ovvero una mini raffineria in ogni veicolo circolante.
Per quanto ardua questa seconda strada potrebbe nel medio termine rappresentare la soluzione da perseguire poiché sarebbe totalmente compatibile con l'attuale rete di distribuzione dei combustibili per l'autotrazione.
Le maggiori difficoltà riscontrate nelle realizzazioni finora eseguite sono legate alle forti differenze che esistono nella composizione delle benzine commerciali e soprattutto all'abbattimento del monossido di carbonio che, come più volte ripetuto, rappresenta un ostacolo al corretto funzionamento della cella.
4.2 Trattamento del combustibile
Attualmente l'unico modo per produrre l'idrogeno in grosse quantità ed in modo economico consiste nell'estrarlo da un idrocarburo tramite un processo termochimico che porta alla rottura dei legami tra carbonio ed idrogeno.
Il tipo processo dipende sia dal tipo di combustibile che dalla tecnologia delle celle; quest’ultima determina quali componenti sono desiderabili e accettabili nel combustibile processato. Per esempio il combustibile mandato in una PEMC deve essere ricco di idrogeno e con un contenuto di CO inferiore a 100 ppm mentre né le MCFC né le SOFC presentano questo problema.
Trattamento del Gas Naturale: il metano comunemente distribuito tramite la rete commerciale contiene degli odoranti a base di zolfo (mercaptani, disulfiti ) per l’individuazione delle perdite. Dal momento che né le celle né il catalizzatore tollerano lo zolfo, questo deve essere rimosso (generalmente con degli ossidi di zinco). Il gas naturale viene normalmente convertito in H2 e CO2 in un reattore per lo steam-reforming. Il reforming con il vapore è il processo che conduce alla più alta percentuale d’idrogeno. Le reazioni di base per il metano e un generico idrocarburo sono le seguenti:
CH4+H2O«CO+ 3H2
CnHm+n H2O« nCO +(m/2+n) H2
CO+ H2O«CO2 + H2
Lo steam reforming può essere utilizzato anche con idrocarburi leggeri come butano e propano. Le reazioni sono endotermiche e richiedono un’ingente quantità di calore. Spesso il combustibile residuo in uscita dalla cella viene bruciato per questo scopo. La temperatura di processamento è compresa tra 760°C e 980°C.
Anche un reformer ad ossidazione parziale può essere utilizzato per convertire combustibili gassosi, ma produce meno idrogeno (circa il 75% di uno steam reformer). Di solito questa tecnica viene usata solo per i combustibili liquidi. Per il metano la reazione di ossidazione parziale è:
CH4+1/2O2«CO+2H2
Trattamento di combustibili liquidi: i combustibili liquidi possono essere trattati in reformers ad ossidazione parziale. Tutti i reattori di ossidazione parziale utilizzano l’ossidazione del combustibile con ossigeno in presenza di vapore; la temperatura e la presenza di catalizzatori dipendono dal tipo di reattore. Per il pentano la reazione è la seguente:
C5H12+5/2 O2 «5CO + 6H2
La reazione complessiva è esotermica e fortemente dipendente dalla temperatura.
Trattamento del metanolo: il metanolo si presta facilmente ad essere riformato sia tramite steam reforming che per ossidazione parziale, di seguito vengono rappresentate le due reazioni:
2H3COH + H2O « 5H2 + CO + CO2
2H3COH
+ O2« 3H2 + CO + + CO2+ HO2
Trattamento del carbone: ci sono numerosi sistemi disponibili che possono essere classificati in tre tipi: a letto mobile, fluido, fluido circolante; tutti questi tre sistemi utilizzano aria o ossigeno e vapore per ossidare parzialmente il carbone e ottenere del gas. Il calore richiesto dal gassificatore è fornito dall’ossidazione parziale del carbone. Nel complesso la gassificazione è un processo esotermico, quindi sono previsti spesso dei sistemi di recupero del calore. La temperatura e la composizione del gas prodotto sono dipendenti dalla quantità di ossigeno e vapore e dal tipo di gassificatore impiegato. Tipicamente vengono prodotti dei contaminanti che devono essere eliminati prima di entrare nel catodo.
Anche altri combustibili solidi come le biomasse possono essere utilizzati dalle celle a combustibile, purché il gas prodotto rispetti le esigenze di purezza della cella. Il sistema risultante sarebbe molto simile ad un sistema con gassificazione del carbone.
Nelle realizzazioni pratiche spesso avvengono contemporaneamente entrambe le reazioni in proporzione tale che il calore necessario per lo steam reforming derivi da quello proveniente dall'ossidazione parziale. Questo tipo di processo prende il nome di autothermal reforming.
Tuttavia se la cella è destinata ad applicazioni stazionarie, in cui non vi sono problemi di spazio, il reforming a vapore del combustibile è senz’altro preferito per la maggiore quantità di idrogeno prodotta; per applicazioni destinate alla trazione si ricorre anche al processamento ad ossidazione parziale, per i seguenti motivi:
· velocità di reazione superiore di un ordine di grandezza, cui corrispondono dimensioni inferiori di un ordine di grandezza;
· reazione esotermica, che non ha bisogno di bruciare combustibile per sostenersi;
· maggiore flessibilità nella scelta del combustibile.
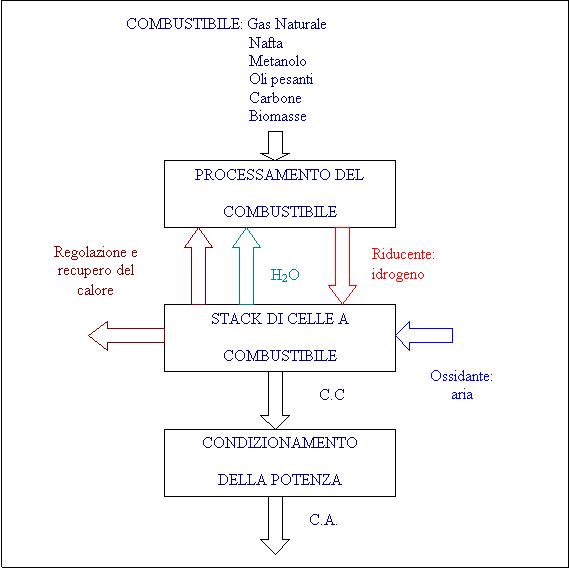
Fig. 1.4-
Schema a blocchi di un sistema con celle a combustibile.
4.3 Impianti di trattamento del combustibile
Numerose sono le ditte che da anni stanno compiendo studi per riuscire a realizzare un dispositivo compatto ed efficiente da poter installare su un veicolo, nel precedente capitolo sono stati evidenziati i parametri individuati dal PNGV per il successo commerciale dei sistemi di processamento on board; si analizzeranno ora le scelte compiute dalle stesse per individuare quale possa essere la tipologia ed il combustibile primario che più facilmente porteranno alla realizzazione di prodotti commerciali.
|
Produttore |
Scelta del combustibile |
steam reforming |
partial oxidation |
|||
|
metanolo |
benzina |
gasolio |
metano |
|||
|
A.D. Little |
2° |
1° |
3° |
|
x? |
x |
|
Daimler Benz |
1° |
2° |
|
|
x |
|
|
General M. |
1° |
2° |
|
|
x |
|
|
Honda |
unica |
|
|
|
x |
|
|
Hydrogen Burner Tech |
|
|
unica |
|
|
x |
|
IFC |
1° |
2° |
|
3° |
x |
x |
|
Johnson Matthey |
1° |
2° |
|
|
x |
x |
|
Mitsubishi |
unica |
|
|
|
x |
|
|
Nissan |
unica |
|
|
|
x |
|
|
Toyota |
unica |
|
|
|
x |
|
|
Wellman CJB |
2° |
1° |
|
|
x |
x |
Tab. 2.4
- Reformer
I risultati riportati nella precedente tabella meritano un'attenta analisi: a differenza delle applicazioni in campo stazionario, molto difficilmente si ricorrerà all'utilizzo del gas naturale per l'estrazione dell'idrogeno. Questa scelta è motivata sostanzialmente da tre ragioni:
· elevata temperatura di processamento del combustibile;
· scarsa disponibilità di una rete di distribuzione per l'autotrazione;
· limitata densità energetica dei sistemi di accumulo.
E' tuttavia importante sottolineare che si prevede uno sviluppo significativo del mercato di veicoli con motorizzazione convenzionale ma alimentati a metano[1], di conseguenza la situazione potrebbe cambiare radicalmente.
Molto probabilmente, quindi, il combustibile primario sarà liquido[2] ma per le ragioni esposte in precedenza utilizzare combustibili commerciali risulta ancora estremamente complicato: da qui nasce l'interesse per il metanolo, un combustibile di sintesi la cui composizione chimica è standard.
Attualmente la produzione mondiale di metanolo è pari al 6% del gasolio consumato nei soli stati uniti d'America e la creazione di impianti per produrlo dal metano in quantità e costi accettabili sarebbe giustificata unicamente per una quantità di autoveicoli superiore a 500.000 unita[3]. Nonostante gli investimenti finanziari richiesti siano consistenti questa scelta è attualmente quella che suscita il maggior interesse dei costruttori.
La figura seguente descrive lo schema blocchi di un reformer per metanolo.
Fig. 2.4- Schema a blocchi di un reformer
per metanolo
Al fine di ridurre la quantità di monossido di carbonio contenuta nel gas riformato esistono dei dispositivi per l'abbattimento dello stesso basati su processi di ossidazione preferenziale (PROX) o di Water gas shift (shift conv.)
4.4 Sistemi di stoccaggio
Qualora la densità energetica dei sistemi di accumulo di idrogeno raggiungesse un valore paragonabile a quello degli idrocarburi si assisterebbe in breve tempo alla definitiva affermazione dell'idrogeno quale vettore energetico ideale.
Le ragioni che portano ad una tale affermazione sono così riassumibili:
- produzione
·
reforming degli idrocarburi con rendimenti elevati e
confinamento della CO![]() ;
;
· fonti rinnovabili: elettrolisi tramite pannelli fotovoltaici, sistemi di pompaggio di centrali idroelettriche, biomasse;
· fotolisi;
·
solar reformer da
![]() [4];
[4];
·
generatori di calore nucleare, Energy Amplifier, da ![]() [5].
[5].
- utilizzo
· tecniche convenzionali di combustione
· bruciatori catalitici
· CELLE A COMBUSTIBILE
Le attuali tecnologie per lo stoccaggio dell'idrogeno sono, tuttavia, ancora lontane dal poter essere considerate paragonabili ai combustibili tradizionali anche se notevoli sono stati i progressi compiuti negli ultimi venti anni.
4.4.1 Serbatoi in pressione
Secondo l'immaginario comune per recipiente in pressione si intende una pesante bombola cilindrica di acciaio o al più di lega di alluminio il cui grado di affidabilità è spesso discutibile.
Attualmente le proposte del mercato sono assai variegate, è possibile scegliere il materiale, la dimensione e la forma del serbatoio desiderato; si può eseguire la seguente classificazione in ordine di densità energetica immagazzinabile, e quindi anche di costo:
1. Bombole cilindriche in materiale metallico, pressione ammissibile » 200 bar
2. Bombole cilindriche in materiale composito, pressione ammissibile » 200¸250 bar
3. Bombole cilindriche in materiale composito avanzato, pressione ammissibile » 345 bar
4. Bombole in materiale composito avanzato con geometria differente da quella cilindrica, pressione ammissibile » 345 bar
La figura seguente mette in evidenza come la possibilità di
conformare la geometria del serbatoio possa far guadagnare nel rapporto tra H![]() immagazzinato e volume del serbatoio stesso aspetto
particolarmente delicato nella trazione automobilistica.
immagazzinato e volume del serbatoio stesso aspetto
particolarmente delicato nella trazione automobilistica.
Fig. 3.4
- Confronto tra le tecnologie di
stoccaggio dell'idrogeno
L'ellissoide interamente celeste mette in evidenza il miglioramento della densità in peso ottenuto con i materiali compositi, quello in giallo la densità in volume già descritta.
Di alcune di queste tecnologie sono stati riportati degli esempi realizzativi[6]:
-
 la
Lincoln Composites realizza da
diversi anni bombole in composito prettamente per uso automobilistico, il
risparmio in peso rispetto alle equivalenti in acciaio è circa del 70%.
la
Lincoln Composites realizza da
diversi anni bombole in composito prettamente per uso automobilistico, il
risparmio in peso rispetto alle equivalenti in acciaio è circa del 70%.
Questi serbatoi sono realizzati con una tecnologia denominata TUFFSHELLTM in grado di ridurre il rischio di fughe di gas in caso di urto accidentale.
La Lincoln dispone di un catalogo molto fornito, la capienza di ogni singolo elemento può variare da 55 a 400 litri, mentre si può scegliere tra 207 e 248 bar; la geometria è unicamente cilindrica.
Attualmente trovano impiego come serbatoi per il metano ma sono state omologate anche per contenere idrogeno.

-
Al vertice della tecnologia oggi disponibile si collocano le
bombole realizzate dalla Thiokol.
Si tratta di serbatoi in composito realizzati tramite una resina epossidica di nuova concezione denominata TCR™ .
L'aspetto fortemente innovativo consiste nel poter realizzare geometrie specifiche per l'utilizzo finale permettendo un risparmio del volume occupato anche del 50 % rispetto ai serbatoi cilindrici.
La sperimentazione finora condotta su questi dispositivi ha portato esito positivo per quanto riguarda la sicurezza derivante da urto accidentale e da combustione; l'attuale vincolo tecnologico riguarda l'abbattimento dei costi ipotizzando la produzione su larga scala.
La pressione massima ammissibile di 344 Bar, unita al Conformable Storage potrebbe soddisfare le specifiche imposte da PNGV.
4.4.2 Idruri metallici
Il
meccanismo che sta alla base di questa tecnologia è piuttosto semplice: molti
metalli hanno la capacità di assorbire all'interno del loro reticolo
cristallino idrogeno molecolare in condizioni di temperatura e pressione
prossime a quelle standard.
La reazione che sta alla base del processo è la seguente:
![]()
Purtroppo
la reazione è lontana dal valore stechiometrico, ne deriva quindi un
pessimo rapporto tra il peso di
idrogeno immagazzinato e il peso della lega metallica.
La situazione è diametralmente opposta se si considera la densità in volume già oggi paragonabile ai serbatoi per idrogeno liquido.
Qualora questa tecnologia raggiungesse il goal desiderato garantirebbe il maggior margine di sicurezza tra tutti i sistemi di stoccaggio.
 4.4.3 Nanofibre di carbonio
4.4.3 Nanofibre di carbonio
La tecnologia dell'assorbimento di gas su solidi si trova ancora allo stato embrionale, potenzialmente la densità di energia, sia in peso che in volume, è paragonabile a quella dell'idrogeno liquido ma la l'efficienza del sistema di rifornimento è enormemente superiore.
I risultati finora ottenuti possono essere così riassunti:
- Peso H![]() / peso fibra = 4.2 %
(pressione = 100 bar)
/ peso fibra = 4.2 %
(pressione = 100 bar)
4.4.4 Idruri salini
Gli idruri dei metalli alcalini e alcalino-terrosi presentano la caratteristica di reagire con l'acqua dando origine ad idrogeno ed all'idrossido del metallo di partenza.
La reazione è veloce e fortemente esotermica ed è necessario un attento controllo del processo per scongiurare il rischio di esplosione. Nel caso dell'idruro di Sodio la reazione è la seguente :
![]()
La densità energetica di questo tipo di dispositivi è estremamente elevata essendo prossima a quella dei combustibili tradizionali[7].
Esistono tuttavia delle motivazioni che rendono ancora dubbia la riuscita di questa tecnologia:
· pericolo di esplosione;
· complessità impiantistiche;
· necessità di produrre l'idruro da combustibili tradizionali con un aggravio nel bilancio energetico.
Riuscendo a rendere il processo semplice e sicuro si tratta
quindi di introdurre due ulteriori passaggi nella conversione dell'energia
chimica del combustibile in idrogeno puro ovvero ![]() . Bisogna inoltre prevedere la raccolta, lo stoccaggio ed il
riciclo dell'idrossido prodotto durante la reazione.
. Bisogna inoltre prevedere la raccolta, lo stoccaggio ed il
riciclo dell'idrossido prodotto durante la reazione.
Si tratterebbe in definitiva di elaborare un vettore energetico intermedio tra un idrocarburo e l'idrogeno. Nonostante queste considerazioni questa strada continua ad essere investigata per le elevate potenzialità di cui dispone.
Dal punto di vista realizzativo esistono due possibilità:
1. Immagazzinare piccole quantità di idruro in sfere polimeriche da far reagire in modo controllato con acqua (Power Ball);
2. Utilizzare una sostanza organica[8] per trasportare particelle di idruro da un serbatoio principale al sito di reazione con l'acqua.
Entrambi gli approcci hanno dimostrato di poter condurre al successo, sono attualmente in fase di sperimentazione le sostanze riportate di seguito:
|
Idruri salini |
||
|
Sostanza proposta |
Wh/kg |
Wh/litro |
|
NaH[9] |
1030 (solo idruro) |
|
|
LiH |
5050 |
2430 |
|
CaH |
2670 |
2430 |
|
NaBH |
4760 |
2570 |
|
LiBH |
6350 |
2640 |
Tab. 3.4
- Idruri salini
Le illustrazioni seguenti mostrano un esempio di questa tecnologia realizzato dalla Power Ball technologies utilizzando idruro di Sodio contenuto appunto in sfere di polimeriche.
Schema
di processo
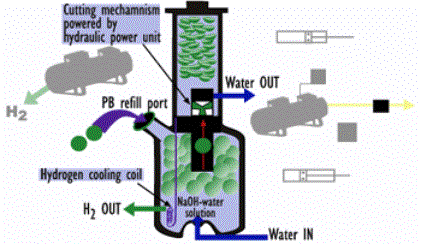
Esempio
di realizzazione
4.4.5 Idrogeno liquido
L'idrogeno può essere reso liquido unicamente ad una temperatura di circa 22 K e quindi con una consistente spesa energetica; una volta liquefatto esistono diverse procedure per mantenerlo in questo stato, ma tutte comportano una spesa energetica.
Questa tecnologia trova un ottimo campo di applicazione in campo aerospaziale dove le condizioni operative sono sensibilmente differenti rispetto alla trazione. Sono stati anche realizzati diversi dispositivi da installare sui prototipi di veicoli elettrici azionati da celle a combustibile ma, sebbene le prestazioni siano dello stesso ordine di quelle dei combustibili tradizionali, le complicazioni impiantistiche che ne derivano portano ad escludere una possibile applicazione commerciale degli stessi.
4.5 Considerazioni progettuali
Al fine di poter realizzare un veicolo sperimentale le possibili scelte oggi praticabili per disporre dell'idrogeno necessario per alimentare il sistema celle sono vincolate dall'insieme dei parametri descritti in questo paragrafo, essi possono essere elencati in ordine di priorità:
· sicurezza;
· elevata densità energetica in rapporto al volume;
· elevata densità energetica in rapporto al peso;
· costo assimilabile agli standard del mercato automobilistico;
· efficienza energetica complessiva.
Nel caso specifico si è deciso di utilizzare un serbatoio in pressione realizzato dalla Lincoln, si tratta di un prodotto realizzato in serie e destinato allo stoccaggio di gas naturale per l'autotrazione, tra i criteri di scelta si è tenuto conto anche del rapporto qualità/prezzo secondo i requisiti appena descritti.
Le caratteristiche del prodotto sono riportate nella tabella seguente:
|
Tuffshell Tank |
|
|
Materiale |
Composito |
|
Dimensioni |
348 x 1016 mm |
|
Peso |
30,9 kg |
|
Volume |
64,8 litri |
|
Pressione |
207 Bar |
Tab.4.4
- Serbatoio idrogeno